
Форма обратного звонка
наши специалисты свяжутся с Вами в ближайшее время


Эта статья основана на практическом опыте работы. В связи с этим, хочу выразить благодарность действующим консультантам проекта "GDPПуть" из России, Казахстана, Узбекистана за участие в написании статьи, предоставление информации о методиках, отзывов клиентов, а также за внимание к важности и необходимости освещения данной темы.
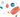
Организация процесса валидации и квалификации дистрибьютора фармацевтической продукции в соответствии с требованиями GDP.


Автор статьи Алексей Хилюк
Участник проекта GDPПуть
В данной статье мы разберем не методики валидации или какие-то конкретные примеры проведения работ по валидации и квалификации, а то, как в соответствии с нормативными требованиями организовать процесс валидации и квалификации в рамках системы качества дистрибьютора.
Поскольку процесс валидации и квалификации является обязательным процессом системы качества дистрибьютора согласно требованию GDP (Good distribution practice), то прежде всего необходимо обратить внимание на определения и требования, указанные в правилах GDP.
В настоящей статье мы взяли за основу требования Правил надлежащей дистрибьюторской практики, утвержденных решением от 3 ноября 2016 г. N 80 Советом евразийской экономической комиссии.
Для начала давайте рассмотрим определения терминов валидация и квалификация Правилах GDP:
- "валидация" - документально оформленные действия, доказывающие, что процедура, процесс, оборудование, материал, операция или система соответствуют заданным требованиям и их использование будет постоянно приводить к результатам, соответствующим заранее установленным критериям приемлемости;
- "квалификация" - документально оформленные действия, удостоверяющие и подтверждающие, что оборудование или вспомогательные системы смонтированы должным образом, правильно функционируют и действительно приводят к ожидаемым результатам.
Теперь обратим внимание на то, что написано в пункте 50 Правил GDP: «Организация должна определить ключевое оборудование и процессы, которые подлежат квалификации и (или) валидации с целью подтверждения надлежащего монтажа и эксплуатации. Объем проводимых работ по квалификации и (или) валидации (например, хранение, подготовка к отгрузке и упаковка) определяется на основе документально оформленного анализа рисков.»
Из этого требования становится ясно, что валидация и квалификация — это не просто документально оформленные тесты, подтверждающие, что какой-либо процесс или оборудование соответствуют заданным требованиям или должным образом функционируют. Валидация и квалификация — это необходимый процесс системы качества дистрибьютора, связанный с другими процессами (например, процессом управления рисками), и при правильной организации которого, наряду с другими процессами, система качества будет функционировать эффективно.
Итак, раз валидация и квалификация — это процесс системы качества, то следует поступать с ним в соответствии с требованиями Правил. Об этом написано в пункте 7: «Система качества должна быть полностью документирована, ее эффективность должна подвергаться мониторингу и анализу. Действия персонала, относящиеся к системе качества, должны быть описаны в соответствующих письменных процедурах…»
Следовательно, в организации необходимо разработать и внедрить в работу стандартную операционную процедуру (СОП), в которой будет определен порядок планирования, подготовки и проведения валидации и квалификации процессов и оборудования дистрибьютора. Именно в СОП, как внутреннем инструменте управления процессом, определяются действия сотрудников в части организации, исполнения и контроля до получения заданного результата. Поэтому разработка СОП является основополагающим этапом в организации процесса валидации и квалификации дистрибьютора.
Для того чтобы описание действий в СОП было понятно исполнителям процесса и его организаторам, описываемый процесс лучше разбить на последовательные этапы. На рисунке 1 вы можете видеть пример такой разбивки.

Рисунок 1

Процессы, помещения, системы и оборудования

Валидированные и (или) квалифицированные процессы, помещения и оборудования

Оценка и оформление результатов проведенной квалификации и (или) валидации

Подготовка и проведение квалификации и (или) валидации
Планирование квалификации и (или) валидации






Мы не будем детально разбирать, как описывать процесс в СОП. Эту тему мы подробно раскроем в другой статье, посвящённой разработке СОП. В данной статье мы обратим внимание на то, что должно быть включено в СОП, описывающую процесс валидации и квалификации, с целью его эффективной организации.
Как видно на рисунке 1, описываемый процесс разделен нескольких основных этапов:
1) Планирование квалификации и (или) валидации;
2) Подготовка и проведение квалификации и (или) валидации;
3) Оценка и оформление результатов проведенной квалификации и (или) валидации.
При этом в начале схемы овальной фигурой обозначен «вход» процесса, то есть то, что необходимо для начала процесса – это процессы, помещения, системы и оборудование дистрибьютора. В конце схемы обозначен «выход» процесса, то, что организация получает в результате его реализации – валидированные и квалифицированные процессы, помещения, системы и оборудование.

Рассмотрим 1-й этап - планирование валидации и квалификации.
На этом этапе важным и первым шагом является определение процессов и оборудования, подлежащих валидации и квалификации. Это требование указано в пункте 50 Правил GDP, на который мы уже ссылались ранее: «Организация должна определить ключевое оборудование и процессы, которые подлежат квалификации и валидации…»
Для того чтобы не упустить из виду оборудование и процессы, требующие квалификации и валидации, необходимо обратить внимание на требования Правил GDP, провести анализ рисков, а также учесть рекомендации Всемирной организации здравоохранения (ВОЗ).
В Правилах GDP, в пункте 44., перечислено наиболее значимое оборудование дистрибьютора, то есть то, которое может оказывать влияние на сохранение качества лекарственных средств: «…К наиболее значимому оборудованию относятся кондиционеры, холодильные камеры (холодильники) или устройства, охранная и пожарная сигнализация, системы контроля доступа, вентиляционная система, система увлажнения и осушения воздуха, термогигрометры (психрометры) или иное оборудование, используемое для регистрации температуры и влажности, а также оборудование, используемое для транспортировки.» Все вышеперечисленное оборудование подлежит квалификации и валидации, кроме средств измерений, которые подлежат поверке и калибровке. Также в пункте 5 Правил GDP, написано о необходимости процессов: «…Ключевые этапы процесса оптовой реализации (включая наиболее значимые изменения) должны быть обоснованы и при необходимости валидированы…». А в пункте 44. GDP установлены требования к валидации компьютеризированных систем: «Перед началом использования компьютеризированной системы необходимо продемонстрировать с помощью валидации или верификации, что система способна получать заданные результаты точно, единообразно и воспроизводимо».
В Рекомендациях ВОЗ в приложении 9, дополнении 7 «Квалификация зон хранения с контролируемой температурой», в пункте 2.2.1 указано следующее: «Все оборудование и системы с контролируемой температурой, используемые для обработки, хранения и распределения термолабильных лекарственных средств должны быть квалифицированны».
Необходимо провести анализ рисков, связанных с влиянием процессов и используемого оборудования на сохранение качества лекарственных средств, чтобы уточнить перечень процессов и оборудования, подлежащих квалификации и валидации.
На основании этого перечня можно приступать к составлению плана-графика проведения работ по валидации и квалификации. План-график, как правило, является неотъемлемой составляющей организации процесса квалификации и валидации. Он обычно содержит следующую информацию:
- наименование объекта квалификации или валидации согласно ранее составленному перечню процессов и оборудования;
- сроки проведения мероприятий по квалификации и валидации по каждому объекту;
- исполнителей работ.
Здесь стоит отметить, что исполнителями работ по квалификации или валидации могут быть как компетентные в этих вопросах сотрудники дистрибьютора или аутсорсера (например, если складская обработка или транспортировка переданы на аутсорсинг), так и внешняя подрядная организация.
Важно отметить, что не нужно путать план-график проведения квалификации и валидации с планом конкретных действий по квалификации или валидации и их описанием, это два разных документа.
Следует также учитывать, что если мероприятия по квалификации и валидации будут проводиться подрядной организацией, то всю валидационную документацию (план квалификации, методики, протоколы, отчёты и пр.) обычно предоставляет эта подрядная организация. Если же мероприятия по квалификации и валидации планируется проводить своими силами, необходимо запланировать подготовку всей валидационной документации, за что обычно отвечает специально обученная группа сотрудников.
На первом этапе планирования осуществляется:
- подготовка перечня процессов и оборудования, подлежащих квалификации и валидации;
- разработка плана-графика проведения мероприятий по квалификации и валидации;
- определение исполнителей мероприятий по квалификации и валидации.
При описании этого этапа в СОП необходимо указать ответственных лиц за исполнение всех действий, лиц, согласующих и утверждающих документы, а также лиц, ответственных за контроль исполнения указанных действий.

2-й этап - подготовка и проведение квалификации и (или) валидации.
На данном этапе необходимо определить все необходимые действия для проведения мероприятий по квалификации и валидации. Объем подготовительных работ и, соответственно, действий, которые необходимо указать в СОП, зависит от того, чьими силами (сотрудниками дистрибьютора или подрядной организацией) будет проводиться квалификация и валидация в каждом конкретном случае.
Если работы будут проводиться собственными силами, то в СОП необходимо предусмотреть этап разработки методики проведения работ по квалификации и валидации. Как разработать эффективную методику для проведения валидации или квалификации – это тема уже другой статьи. Важно, чтобы сотрудники, участвующие в разработке документации, методики и проведении валидационных работ, обладали достаточными компетенциями для выполнения этих действий. Все разработанные методики проведения квалификации и валидации, а также оборудования и процессов, используемых дистрибьютором для осуществления своей деятельности, могут быть приложены или описаны в инструкциях к СОП по квалификации и валидации. Таким образом, будет обеспечена прослеживаемость регламентирующей документации в системе качества.
В случае, когда нанимается подрядная организация для выполнения работ по валидации и квалификации, необходимо предусмотреть мероприятия по оценке и выбору подрядной организации. Таким образом, прослеживается взаимодействие процессов оценки и выбора поставщиков услуг с процессом квалификации и валидации в системе качества. Как правило, в СОП по квалификации и валидации указывается ссылка на СОП по оценке и выбору поставщиков услуг, в соответствии с которым определяются четкие критерии оценки подрядчика. И, конечно, с выбранной подрядной организацией необходимо заключить договор на оказание услуг, что тоже должно быть определено процедурой.
В случае привлечения подрядной организации, обычно разрабатывают всю документацию и проводят все работы специалисты подрядчика под наблюдением представителя дистрибьютора. Проведение работ по квалификации и валидации может использоваться как на постоянной основе, так и разово, например, когда необходимо уложиться в установленные сроки или набраться опыта.
Следует отметить, что если работы по квалификации и валидации проводит подрядная организация, то сотрудникам дистрибьютора, отвечающим за организацию данного процесса, необходимо в полной мере понять и разобраться в методиках и специфике проводимых действий подрядчиком.
При описании этого этапа в СОП необходимо указать ответственных лиц за исполнение всех действий, лиц, согласующих и утверждающих документы, а также лиц, ответственных за контроль исполнения указанных действий.

3-й этап - оценка и оформление результатов проведенной квалификации и (или) валидации.
На данном этапе определятся действия, связанные с оформлением результатов проведенной квалификации и валидации, а также действия, в случае если при проведении квалификации или валидации были выявлены отклонения.
Если квалификация и валидация проводится своими силами, то в СОП необходимо определить порядок оформления результатов, например, анализ полученных данных и оформление заключения, формирование отчета о всех отклонениях выявленных в процессе проводимых работ, оформление итогового отчета с выводами и рекомендациями.
Если квалификация и валидация проводится подрядчиком, то предусмотреть действия по принятию и проверки валидационных документов, предоставленных подрядчиком.
О необходимости оформления данных в виде отчетов написано в пункте 50. GDP: «Проведение валидации или квалификации оформляется отчетами, в которых должны быть обобщены полученные результаты, а также даны объяснения выявленным отклонениям.»
Также на этом этапе нужно предусмотреть разработку корректирующих и предупреждающих действий САРА (от англ. Correctiveand Preventive Action), если были выявлены отклонения, эти требования установлены в пункте 51. GDP: «Отклонения от установленных процедур документально оформляются, разрабатываются меры, направленные на их устранение, а также на предотвращение их появления в будущем (корректирующие и предупреждающие действия)…». Как правило, если говорить об описании действий в СОП, то в СОП по квалификации и валидации указывается ссылка на СОП САРА, в котором подробно определены действия сотрудников.
После реализации САРА, проводятся при необходимости дополнительные мероприятия по квалификации или валидации до тех пор, пока не будут получены удовлетворительные результаты, соответственно эти действия также должны быть предусмотрены в СОП и формах для записей. Требования на счет это указаны в п 51. GDP «…Должны быть получены доказательства успешной валидации и приемлемости процесса или оборудования, которые утверждаются соответствующими работниками.».
В завершении рекомендую уставить ключевые показатели оценки процесса квалификации и валидации, потому как процессы необходимо не только определить и описать в СОП, но ими нужно еще и управлять. Здесь будет уместно примести слова известного предпринимателя Джека Уэлча: «Что невозможно измерить, тем невозможно управлять.». Показатели оценки процесса квалификации и валидации дистрибьютора могут включать следующие аспекты:
- Своевременность проведения квалификации и/или валидации.
- Наличие и полнота отчетов по квалификации и/или валидации.
- Своевременное реагирование на отклонения по результатам квалификации и/или валидации.
После определения этих показателей их необходимо количественно оценить, установив плановые значения, такие как дни, часы, количество инцидентов, финансовые затраты и другие параметры, соответствующие каждому показателю. Определение измеримых показателей является важным аспектом с точки зрения GDP. В требованиях к процессу анализа со стороны руководства, указанных в пункте 13 GDP, говорится: «Руководство организации должно установить формализованный процесс периодического обзора системы качества. Обзор должен включать в себя: … б) оценку показателей эффективности, которые могут быть использованы для мониторинга эффективности таких процессов системы качества, как количество претензий, отклонений от установленных норм, эффективность корректирующих и предупреждающих действий, изменения в процессах, отзывы о деятельности по аутсорсингу, процессы самопроверки (включая анализ рисков и аудиты), результаты внешнего контроля (включая инспекции и аудиты), выявленные несоответствия, аудиты клиентов;...».
Искренне надеемся, что информация в этой статье будет полезна и поможет более эффективно организовать процесс квалификации и валидации в системе качества у дистрибьюторов фармацевтической продукции.
Если у вас возникнут вопросы или вы захотите обсудить что-либо более детально, пожалуйста, не стесняйтесь связаться с нами по электронной почте: Info@gdpway.com. Мы будем рады помочь вам!
С Уважением к Вам, Алексей Хилюк
Остались вопросы? мы Вам перезвоним


